本期分享MichaelL.Perlis于2001年在sleep杂志上发表的一篇文章,题为Beta/GammaEEGActivityinPatientswithPrimaryandSecondaryInsomniaandGoodSleeperControls的文章。
摘要:
研究目的:几项研究表明,失眠患者在睡眠发作时或睡眠前后以及在NREM睡眠期间表现出较高水平的β-EEG活性(14-35Hz)在这项研究中,我们评估了:1)高频脑电活动被限制在14-32Hz域的程度,2)高频脑电活动(HFA)是否与睡眠连续性的主观和PSG量度之间的差异有关,以及3)相对于继发性失眠,原发性失眠患者发生高频脑电活动的程度。
设计:比较三组(每组n=9):原发性失眠,继发于严重抑郁的失眠和良好的睡眠者控制。
根据年龄,性别和体重对组进行匹配。
在去除清醒和运动时期以及包含醒或微运动的时期之后,为每个NREM周期创建平均光谱图。
地点:睡眠研究实验室。
患者或参与者:原发性和继发性失眠患者。
干预措施:N/A
测量和结果:与其他两组相比,原发性失眠患者的Beta-1(14-20Hz),Beta-2(20-35Hz)和Gamma活性(35-45Hz)表现出更高的平均NREM活性(p<01)。
组间差异也暗示了欧米茄的活动(45.0-125Hz)(p.<.10),其中MDD受试者倾向于表现出比其他组更多的活动。
相关分析表明,平均NREMBeta-1和Beta-2活性与总睡眠时间和睡眠潜伏期的主观-客观差异测量值呈负相关。
结论:我们的结果证实,β活性在原发性失眠中增加。
此外,我们的数据表明,原发性失眠患者的高频活动仅限于Beta/Gamma范围(14-45Hz),并且与睡眠感呈负相关。
关键字:失眠;功率谱分析;睡觉;Beta;高频脑电图
前言:
20-90HZ中的高频脑电活动范围是1937年BERGER首次观察到的。
他假设在心算过程中观察到的这种活动一定是“心理过程的物质伴随”。
在过去的二十年中,有大量的工作表明Beta中的高频EEG活动(14-35Hz)和更可能是在Gamma(35-45Hz)中,范围与动物的注意力2,3有关,与人类的注意力,知觉以及更普遍的认知功能有关。
最近,有六项研究表明,失眠患者在多导睡眠图(PSG)监测的睡眠过程中表现出异常的βEEG活性。
这些研究中的大多数发现,失眠患者的β活性(14-35Hz)明显增加与良好的睡眠者对照相比,在睡眠发作前后/和/或NREM睡眠期间为。
基于1)使用单极性或双极性测量方法(包括C3,Cz或C4)从中心站点进行的脑电图测量,以及2)相对于绝对功率测量的相对(相对于绝对)测量。
在中央脑电图位置的β活性检测表明,这种形式的脑电图活性可能最大程度地分布在与感觉过程相关的区域上。
使用相对量度(相对于功率密度的绝对量度)对Beta活性的检测表明,这种形式的EEG可能特别容易出现个体差异变异性。
Beta活动研究的结果很直观,吸引人的一方面是因为它们与失眠的心理概念一致,另一方面是因为它们提供了关于症状,认知过程和潜在的神经生理学之间可能联系的观点。
Beta的发现与心理数据表明的一致
失眠患者可能会在入睡时和/或入睡时表现出过度警觉和/或反刍作用。
Beta测试结果使他们对失眠的病理生理学有了更清晰的认识,因为他们指出了过程(感觉和信息处理,注意力,长期记忆)和暗示的结构(丘脑,感觉皮层,前额叶皮层,海马等),可能与睡眠引发和维持问题有关。
PSG睡眠期间的活动水平,关于失眠的高频脑电图活动是否为以下情况知之甚少:
1)限于Beta活动(14-35Hz)或作为认知神经科学文献建议将其扩展到EEG频谱的Gamma部分(35-45Hz)。
2)实际上是CNS的起源。
Beta和伽马射线活动是EMG人工产物的形式,因此代表了与CNS相反的体细胞唤醒。
3)简单的微体系结构现象的派生,例如增加“唤醒”的次数和/或持续时间(事件在每个时期的持续时间少于15秒)。
4)与睡眠质量和数量的主观感知相关。
5)特定于原发性失眠或继发性失眠的特征(例如,与严重抑郁有关的失眠)。
在这项研究中,我们评估了1)高频脑电图活动限制在14-35Hz频域的程度,2)Beta和/或Gamma活性是否与睡眠连续性的主观测量和PSG测量之间的差异相关(即,可以解释失眠症患者相对于多导睡眠监测仪高估了其睡眠问题的严重性的趋势)和3)高频率活动是否主要发生在原发性失眠患者中。
方法
基本方案
这些分析中的所有受试者都参加了罗切斯特大学睡眠研究实验室进行的三个试验研究之一。
从两个来源招募受试者,并按照两级流程进行筛选,以确保他们符合纳入/排除标准。
在进行实验室研究之前,所有受试者均完成了14天的睡眠日记。
这些数据被用来验证受试者对其睡眠的回顾性评估是相当准确的,并提供每个受试者偏爱的就寝时间和起床时间的平均量度。
在两个星期的监视间隔之后,每个受试者在实验室中至少度过了两个连续的晚上。
第一个夜晚是适应夜,这些数据将用于当前分析中。
招募
通过报纸广告和罗彻斯特睡眠障碍中心的行为睡眠医学诊所招募受试者。
每个患者都经历了两个步骤的评估过程。
首先,通过电话采访对象以确定其参加资格。
排除受试者是否报告了不稳定的医疗疾病,除重度抑郁症以外的精神病,睡眠障碍或暗示除原发性失眠以外的睡眠障碍的症状,轮班工作,使用具有中枢神经系统作用的药物,药物滥用和/或近期酗酒史(两年内)。
电话屏幕显示后,所有潜在受试者都接受了研究临床医生的采访。
使用“情感障碍和精神分裂症-终生精神分裂症时间表”(SADS-L)对受试者进行了访谈,并补充了SCID的进食障碍模块。
还确定症状严重程度(汉密尔顿抑郁量表[HRSD]),病情,治疗,病史以及睡眠障碍的个人和家族病史。
根据家族史研究诊断标准(FHRDC)获得了精神疾病的家族史。
预期受试者还完成了包括贝克抑郁量表,贝克焦虑量表和匹兹堡睡眠质量指数在内的多种心理测量仪器。
受试者获得$150-$200的报酬。
对象
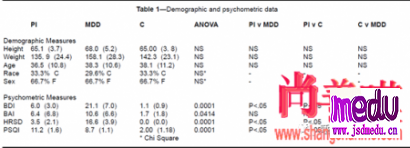
本分析使用了三个受试者组的数据(每组n=9)。
分组为原发性失眠,继发于重度抑郁的失眠和良好的睡眠者控制。
根据年龄,性别和体重对这三组进行匹配。
总体样本中女性为66%,平均年龄为37.5(+/-10.7)。
原发性失眠的标准如下:①失眠和白天功能受损的投诉;②表示已学会防止睡眠的关联;③积极寻求帮助。
失眠主诉具有以下一项或多项特征:入睡时间超过30分钟和/或觉醒时间>15分钟的觉醒时间>2次和/或睡眠发作时间>30分钟后醒来的时间,问题频率>4周/周,问题持续时间>6个月。
重度抑郁(MDD)继发失眠的标准如下:患者达到MDDF的DSMIV标准或更高的症状(至少从过去的两周开始表现出功能改变),情绪低落和/或兴趣/愉悦感丧失用于诊断患有失眠症的MDD患者。
良好睡眠习惯(GS)的标准是:表示没有困难入睡或保持睡眠;将他们的睡眠描述为恢复性和相对稳定的。
所有3组的排除标准是:1)除单相抑郁症以外的重大当前医学或精神疾病;2)除原发性失眠以外的睡眠障碍;3)记忆力减退;4)头部受伤史;5)在四个疗程内使用处方药或娱乐性药物6)在实验室研究的六个月内使用SSRI。
多导睡眠图评估
录制的剪辑画面至少包含15个电生理信号。
基本蒙太奇包括两个以单个乳突[LOC&ROC]为参考的EOG,六个以链接乳突[F3,F4,C3,C4,O1和O2]为参考的脑电图,一个双极mentalisEMG,双侧瓦楞纸肌电图和一个EKG。
另外,获取了两个通道的胫骨EMG和一个通道的鼻/口气流数据,以排除隐匿性睡眠障碍(例如睡眠呼吸暂停和/或PLM)的存在。
所有电生理信号均使用CoulbournInstruments16通道POLYLINC™系统获得。
在初始频率带宽为0.3–100Hz(24dB/倍频程)的情况下,以20K的增益(等效于3.75Uv/mm)获取EOG。
再次以20K的价格获取EMG,初始带宽为30-1000Hz。
在0.3-1000Hz的初始带宽下,以20K的增益获取了EEG。
EEG信号也串联传递到设置为0.5-125Hz的六个库尔本仪器V75-48带通滤波器(48dB/倍频程)。
数字采集由StellateHarmonie-Luna™软件控制,并由BSMI519A-to-Dboard完成。
A-D板具有60Hz的陷波滤波器和300Hz的a1极(6dB/倍频程)低通滤波器。
基本采样率为512Hz。
使用在线抽取,因此可以获得可变的采样率。
根据奈奎斯特频率(采样=2x最高感兴趣频率)计算出的可变采样率如下:EOG为16Hz,EEG为256Hz,EMG为512Hz。
最终的数字显示还通过数字滤波进行了修改,以实现最佳的屏幕显示(不影响定量分析)。
数字带通滤波器设置如下:EOG为0.3-4Hz,EEG为0.3-20Hz,EMG为30-250Hz。
睡眠评分
睡眠评分根据Rechtschaffen和Kales(R&K)标准在30秒内对PSG评分。
我们的评分程序在两个方面与R&K方法和标准略有不同。
首先,我们对K复合物有一个持续时间和幅度标准,基于Bastien等人的工作,50K复合物必须至少为50mV。
其次,根据Dementet等人的早期工作,51如果没有纺锤体和K复合体持续三分钟或更长时间,则可能将第二个时期记为第二阶段睡眠,如果
确定了5-19%之间的Delta活性。
PSG评分员由第一作者进行了广泛的培训,并达到或超过了90%的实验室内部评分者标准。
也就是说,必须标识90%的纪元与由PI评分的五个标准记录的主集合中的纪元相同。
除睡眠评分外,记分员还识别并编码了微型(0.1-7.0秒)和微型(7.1-14.9秒)闹钟。
唤醒被确定为短暂的EEG“加速”,“笔杆阻塞”(放大器饱和)的短时间间隔和/或EMG活动的偶然侵入。
PSG定义如下:睡眠发作定义为阶段1的两个连续时期或阶段2,3,4或REM的1个时期。
觉醒定义为入睡后发生1分钟以上的清醒。
这些定义是StellateHarmonieLuna™报告生成程序的默认值。
根据这些定义,睡眠连续性变量如下:
1)睡眠潜伏期:从数分钟起经过的时间“熄灭”到“睡眠发作”
2)唤醒次数(NUMA):唤醒次数发生在入睡后和“开灯”之前
3)入睡后唤醒(WASO):是唤醒时间的总和从入睡到“开灯”的分钟数,
4)总睡眠时间:以分钟为单位的NREM和REM睡眠之和从“熄灯”到“点亮”。
脑电频率评估
功率谱分析(PSA)是一种统计技术,用于检测时间序列数据中的周期性。
正如脑电图所采用的那样,该技术通常用于将复杂的波形分解为它们的组成频率。
通过确定预定带宽下每Hz出现的电压量,可以完成量化。
使用StellateHarmonie-Luna™软件对1晚起的数字EEG进行了功率谱分析。
在本次分析中,频谱窗口设置为两秒间隔。
在进行频率评估之前,两个秒窗口内的数据会自动进行余弦渐减和去趋势(均值去趋势),以消除非平稳数据。
将重叠的窗口(15/epoch)平均以得出每个睡眠刻划30秒的时间(0.5Hz分辨率)的平均功率谱分布。
针对以下带宽计算每个EEG站点的功率谱(mV2/Hz):Delta-1(0.5-2.5Hz),Theta(2.5-7.5Hz),Alpha(7.5-12.0Hz),Sigma(12-14Hz),Beta-1(14.0-20.0Hz),Beta-2(20-35Hz),Gamma-1(35-45.0Hz)和Omega(45.0-125Hz)。
遵循PSA例程,为每个主题创建了ASCII数据集,该数据集以列格式包含以下项:时间,时期,NREM/REM周期,睡眠阶段,微声事件,微声事件以及八列,其中每个光谱包含绝对功率值。
这些文件已导入SAS。
使用该平台,可以操纵每个受试者的PSA数据,以便:1)唤醒和移动时间纪元以及具有微小(0.1-7.0秒)或微小(7.1-14.9秒。
)唤醒的纪元,2)相对功率值(每带宽的功率超过每个时期每个站点的总功率)。
总功率是通过将每个时期的8个带宽中的每个功率值与3个按站点的平均值(例如C3/A2和C4/A1)和跨站点的平均值([C3/A2+C4/A1]/2)相加得出的计算每个NREM周期。
NREM和REM周期定义如下:
NREM-1被定义为从睡眠发作到第一个REM期。
NREM-2被定义为从第一个REM周期的最后一个时期到第二个REM周期的第一个时期。
NREM-3被定义为从第二个REM周期的最后一个时期到第三个REM周期的第一个时期。
一个REM时期被定义为REMsleep的30秒或更长时间。
REM期被确定为截然不同的-干预NREM睡眠连续15分钟。
最终输出数据表示前3个NREM周期的平均NREM功率(相对功率)。
使用相对功率度量(例如[Beta功率/总频谱功率]*100)来控制1)关于EEG功率的个体差异变异性;2)提供具有直观吸引力的测量单位,即占总百分比大脑活动属于每个给定的频率范围。
分析是有限的到前三个周期,以确保各组之间有可比较的数据。
对于本分析,仅使用平均NREM中央EEG数据([C3/A2+C4/A1]/2)。




讨论
在本研究中,我们发现失眠患者在NREM睡眠期间比具有MDD或良好睡眠者对照的患者表现出更多的Beta-1,Beta-2和Gamma活性,并且明确睡眠期间的Beta活性(12-35Hz)与这种趋势相关低估了总睡眠时间。
为什么组间睡眠连续性影响如此轻微?
至少有两种可能的解释。
首先,本研究的数据是从第一个实验室内研究之夜收集来的。
结果,“第一夜”(睡眠良好的睡眠者睡眠质量较差)和“逆向第一夜”(失眠患者的睡眠睡眠效率较高)的效应可能减弱了群体差异,尤其是MDD和睡眠良好者之间的差异。
其次,在收集数据之后,我们发现允许受试者设置自己的就寝时间和起床时间有无意影响;良好的睡眠者将自己的睡眠时间分配为最短的时间(总床时间[TTIB])。
结果,该小组最有可能增加总睡眠时间的机会并不适合他们。
此问题已通过将TTIB固定为七个小时来解决。
主观-客观上的下降主要发生在失眠患者中吗?
有大量文献表明,失眠症患者往往高估了他们入睡的时间以及相对于PSG措施获得的睡眠量。
尚不清楚的是:1)在包括睡眠次数和持续时间在内的所有睡眠连续性参数上偏差是否一致,以及2)良好的睡眠者和/或继发性失眠的患者表现出相似趋势的程度。
我们的数据表明,偏倚并不均匀,主观客观差异会发生,但睡眠不足者和继发性失眠患者的主观客观差异要少得多。
对我们而言,缺乏统一性非常具有启发性。
这表明失眠患者并不能简单地全面报告其症状更为严重。
因此排除了“神经病”作为所谓的睡眠状态误解的唯一解释。
原发性失眠中的HFA是否仅限于EEG功率谱的Beta部分?
我们的发现与认知神经科学文献相符,表明高频脑电活动不限于Beta范围,而是延伸到EEG谱的Gamma部分。
由于两种形式的脑电活动均与认知功能有关(感觉过程,注意力,知觉知觉和长期记忆),因此这些数据支持以下观点,即失眠的病理生理学部分与无法在睡眠发作前后/NRE睡眠期间脱离认知过程有关。
有趣的是,MDD受试者(虽然很少表现出Beta/Gamma活性)在Omega范围内表现出增强的活性。
如果该范围内的活动是颅面肌电活动增加的主要相关因素,则该发现与以下观点一致:抑郁症与躯体亢奋有关,例如,通过夜间夜间核心体温升高,血浆和尿皮质激素水平升高。
原发性失眠中的HFA是否仅限于EEG功率谱的Beta部分?
我们的发现与认知神经科学文献相符,表明高频脑电活动不限于Beta范围,而是延伸到EEG谱的Gamma部分。
由于两种形式的脑电活动均与认知功能有关(感觉过程,注意力,知觉和长期记忆),这些数据支持以下观点:失眠的病理生理学部分与在NREM睡眠过程中/周围和睡眠开始时无法脱离认知过程有关。
有趣的是,MDD受试者(虽然很少表现出Beta/Gamma活性)在Omega范围内表现出增强的活动。
如果该范围内的活动是颅面肌电活动增加的主要相关因素,则该发现与以下观点一致:抑郁症与躯体亢奋有关,例如,通过夜间夜间核心体温升高,血浆和尿皮质激素水平升高。
原发性失眠中枢神经系统高频脑电活动是否起源?
为了直接解决这个问题,可能需要使用另一种可能不受颅面EMG活性影响的测量策略来显示中枢神经系统激活的增加。
颅内EEG,M-EEG,SPECT或PET是此类评估的理想选择。
我们小组目前正在使用SPECT获取数据。
在没有直接测试的情况下,缺乏欧米茄活性
提供了特异性的证据。
这表明,原发性失眠中发生的Beta和Gamma活性与EMG假象无关。
30如果确实如此,失眠患者在整个功率谱的整个上部都表现出增强的活动。
如果中枢神经系统起源,高频脑电活动是否仅与宏观建筑现象有关(例如,醒来的发作次数和/或持续时间,运动时间和/或“微唤醒”增加)?
这是一个可行的假设,因为一些较早的工作并未详细处理假象排斥问题。
因此,微小和小型唤醒的数量或持续时间增加和/或短暂的清醒发作可能占很小的百分比发生在NREM睡眠的较高频谱。
虽然仍然可能,但我们研究中使用的方法使这种解释的可能性降低。
如前所述,在计算NREM平均值之前,删除了所有带有微或微唤醒的纪元,以及所有记为唤醒或移动时间的纪元。
因此,NREM光谱图完全基于睡眠脑电图。
Beta/Gamma活动是否与睡眠量的主观感知相关?
我们通过检查平均NREMBeta/Gamma活性与睡眠潜伏期(SL),睡眠开始后唤醒时间(WASO)和总睡眠时间(TST)之间的主观客观差异分数之间的整体样本相关性,评估了这个问题。
我们的目的是关注Beta/Gamma活性是否可以解释与无法感知PSG睡眠有关的一些差异。
我们的观点是-明确睡眠中的Beta/Gamma(或与其相关的过程)是否受到干扰在觉察到睡眠的情况下,睡眠时的Beta/Gamma值应与感知睡眠的能力负相关。
与WASO缺乏相关性也是有道理的。
该样本中的所有受试者都没有感知PSG定义的觉醒的困难。
所有三组均准确到+/-5分钟内。
鉴于差异很小在Δ_WASO变量中,并且Beta/Gamma活性存在相当大的差异,因此未检测到显着的相关性。
换句话说,没有主观的客观WASO差异可以解释。
最后,与Δ_SL测度的弱正相关似乎也易于解释。
如果Beta/Gamma活动干扰睡眠感知,则可能会期望这种活动会影响有关睡眠潜伏期的判断。
问题在于Beta/Gamma活性的平均NREM度量值可能与某些离散定义的睡眠发作间隔得出的结果不同,因此,平均NREM度量不太可能反映睡眠发作时β/Gamma活性的强度,因此仅基于Beta/Gamma的睡眠发作水平与平均NREM水平之间的松散相关性,仅产生适度的相关性。
可以预期诸如Merica及其同事使用的测量(例如Delta和Beta斜率和/或它们的相互作用)与睡眠潜伏期的主观客观差异之间存在更强的相关性。
我们的相关发现确实具有启发性,但也令人困惑。
由于β与睡眠总时间的主观-主观差异评分显着相关,并且倾向于与睡眠潜伏期的主观客观差异评分相关,因此该结果具有启发性。
这些发现与失眠的神经认知模式一致,高频脑电活动与干扰睡眠数量和质量感知的过程有关。
29结果令人困惑,因为相关性限于贝塔值范围,且幅度适中(r=-0.46)。
与伽玛活动缺乏相关性向我们表明,而两种形式的活动都被认为与认知过程有关,两个光谱域可能不能平等地代表信息处理的所有组成部分。
例如,Beta-1和Beta-2可能与长期记忆功能相关,而伽玛活动更具体地与感觉处理和注意力有关。
相关程度表明,尽管Beta活动可以解释大量的主观客观差异,但与NREMBeta活动相关的因素以外的因素也构成了“睡眠状态误解”。
结论
累积地,有充分的证据表明,与良好的卧铺控制者和患有继发性失眠的MDD患者相比,失眠患者的Beta/Gamma活性在睡眠发作前后/NREM睡眠期间增加。
也有初步数据表明BetaEEG活性1)为负与患者感知睡眠的能力有关;2)随临床过程而变化。
这些数据的结合表明在该领域的进一步研究将是富有成果的。
可能的方向可能包括脑电图脑电图测定法确定β/γ活性的地形分布,进行脑成像以确定β/γ活性的来源,和/或通过时间生物学研究确定β/γ活性如何在全天24小时内和/或非优先阶段睡眠的各种时间变化。
这些类型的研究,包括多个比较组和/或使用具有治疗成分的纵向研究,是在理解失眠的神经生物学和现象学方面可能最大程度地提供了信息。
参考文献格式:PerlisML,SmithMT,AndrewsPJ,etal.Beta/GammaEEGactivityinpatientswithprimaryandsecondaryinsomniaandgood sleepercontrols[J].Sleep,2001,24(1):110-117.